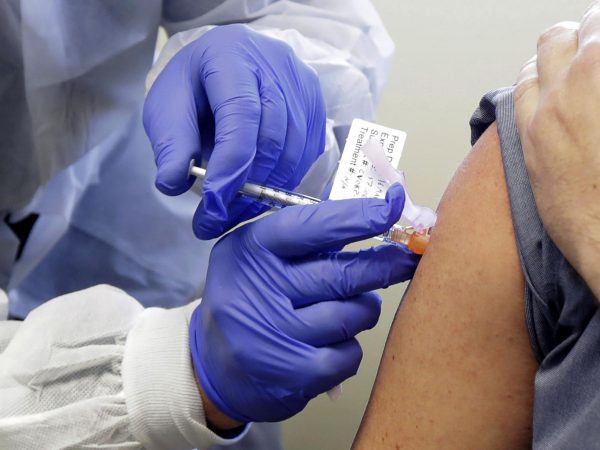
La casa farmaceutica Pfizer prevede di chiedere l’autorizzazione per il suo vaccino anti-Covid la terza settimana di novembre. L’azienda è pronta a richiedere la procedura di emergenza alla Fda statunitense se i dati della sperimentazione di questo mese saranno positivi.
Vaccino covid, la Pfizer annuncia: “Potrebbe essere pronto a novembre”
In Italia è l’immunologo Roberto Burioni a darne notizia. “Albert Bourla, amministratore delegato di Pfizer, in una lettera aperta, ha detto che se tutto andrà bene presenterà una richiesta per un’autorizzazione di emergenza del vaccino contro COVID-19 nella terza settimana di novembre 2020”, spiega sulla sua pagina Facebook.
Burla, in una lettera pubblicata sul sito del gruppo, ha voluto prima di tutto fare chiarezza su quali siano i passi necessari per introdurlo sul mercato.
Anzitutto, il comitato di scienziati indipendenti dovranno comunicare se il trattamento sia efficace, dopo la lettura dei risultati dei test. Prima che possa essere protocollato e poi immesso sul mercato, il vaccino deve superare vari step.
“In primo luogo, il vaccino deve essere dimostrato efficace, il che significa che può aiutare a prevenire la malattia COVID-19 almeno nella maggior parte dei pazienti vaccinati”, spiega Albert Bourla.
“In secondo luogo, e altrettanto importante, il vaccino deve essere dimostrato sicuro, con dati di sicurezza affidabili generati da migliaia di pazienti. Infine, dobbiamo dimostrare che il vaccino può essere costantemente prodotto secondo i più elevati standard di qualità”, ha aggiunto l’amministratore delegato di Pfizer.
La U.S. Food and Drug Administration (Fda) ha richiesto due mesi di dati certi dalla fine della somministrazione su almeno la metà dei partecipanti per garantire l’Emergency Use Authorization (Eua, autorizzazione per uso d’emergenza). “Sulla base dei nostri trial attuali e del ritmo di dosaggio, stimiamo di raggiungere questo traguardo nella terza settimana di novembre”, ha spiegato Bourla.
BioNTech e Pfizer si sono impegnate a fornire oltre 450 milioni di dosi tra la fine di quest’anno e il prossimo anno, a seguito della dimostrazione di efficacia e sicurezza del vaccino e del via libera normativo. Il governo statunitense ha già fatto un ordine iniziale di 100 milioni di dosi con riserva di un acquisto aggiuntivo di 500 milioni di dosi. Invece, l’Unione europea ha ordinato 200 milioni di dosi e potrà acquistarne altri 100 milioni, il Giappone 120 milioni e la Gran Bretagna 30 milioni.